(1)例題
He–, Li2+, Be3+, ……のように1個の原子核とただ1個の電子から構成されるイオンを「水素様イオン」という。水素様イオンはその定常状態の構造が水素原子に類似している。したがって放出される光子の波長スペクトルについても類似性が見られる。
この水素様イオンについて以下の問いに答えよ。ただし、電子の質量をme, 電気素量をe, 真空の誘電率をε0, プランク定数をhとし、必要に応じて次の数値と表のデータを用いよ。
真空中の光速度 c=3.00×108[m/s]
電気素量 e=1.60×10-19[C]
プランク定数 h=6.63×10-34[J・s]=4.14×10-15[eV・s]
水素原子の量子数nに対する定常状態のエネルギーEn
| n | 1 | 2 | 3 | 4 | 5 | 6 | … | ∞ |
| En[eV] | -13.6 | -3.40 | -1.51 | -0.850 | -0.544 | -0.378 | … | 0 |
①以下の文中の空欄に当てはまる適当な式、記号を答えよ。



②ある1種類の水素様イオンから放出される光子を測定したところ、下図のような波長スペクトルが得られた(なお、強度が小さい線も同じ強度に見えるように修正してある)。ところどころにスペクトル線が集中して重なっているが、これはどのような理由によるものか。前問の結果を用いて定性的に説明せよ。
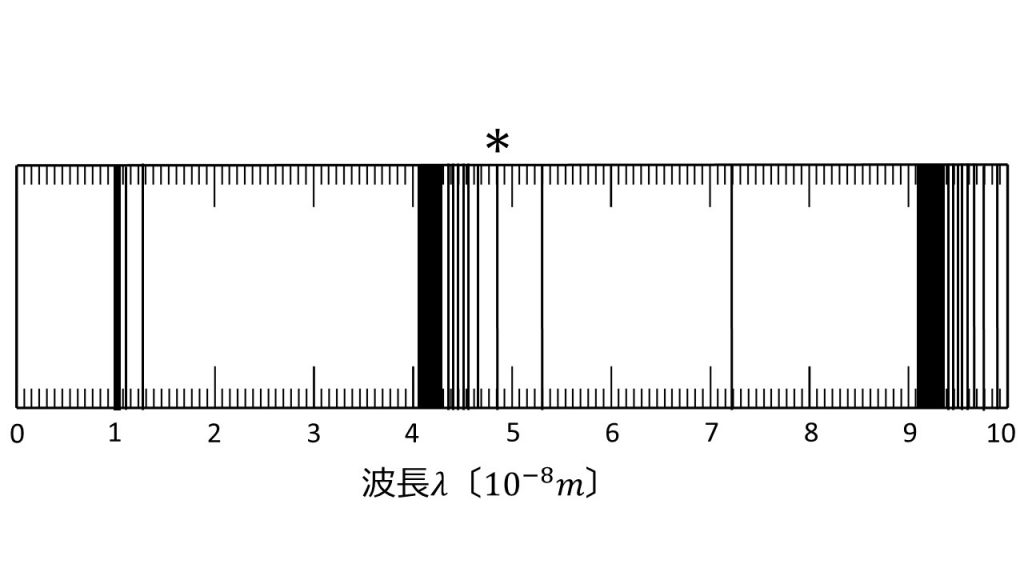
③図のスペクトルからこの水素様イオンの元素名を判定せよ。計算の経過も示すこと。
④図で*を記したスペクトル線は、上で特定されたイオンがどの定常状態からどの定常状態に移るときに放出された光子に対応するものか。量子数で答えよ。
⑤この水素様イオンの量子数n=2の定常状態にあった電子を原子核から完全に引き離し、1個の原子核と1個の自由な電子にするために最低限必要なエネルギー[eV]を求めよ。計算の経過も示すこと。
(東工大入試問題より)
(2)例題の答案
①ア
炭素原子は6個の電子をもつので、水素様イオンとなるのは
C5+
①イ

①ウ


①エ

①オ
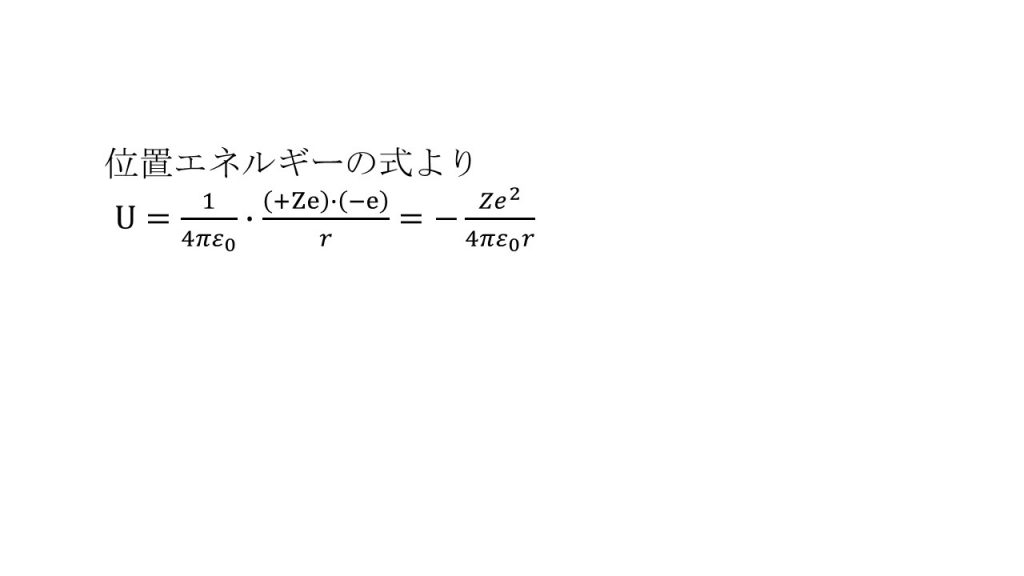
①カ

①キ

①ク

①ケ

①コ

②
①コの式で、mを固定してnを変化させると、nが大きくなればなるほど波長の変化量は小さくなることが分かる。よって、スペクトル線が集中して重なる理由は、
大きな量子数nからの遷移では、nが変化してもあるmへの遷移のときに放出されるエネルギー変化も小さく、波長もあまり変化しないからである。
③
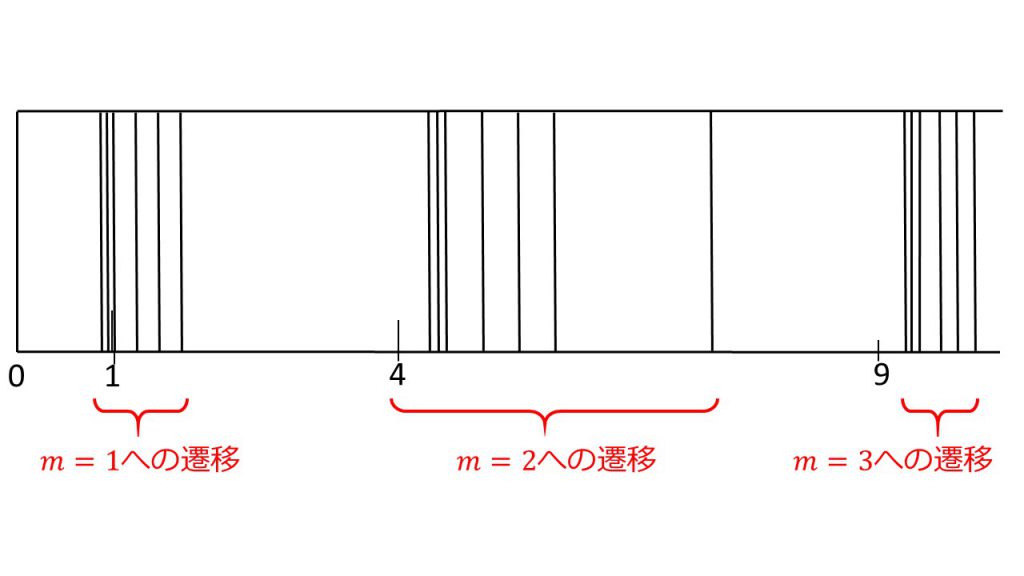

④

*はn=3, 4, 5……のいずれかからm=2への遷移を表す。nが小さいほど放出されるエネルギーは小さく、波長は長くなるので、右からn=3, 4, 5……の順になる。
よって、*のスペクトルは
n=5からm=2への遷移
⑤

(3)解法のポイント
①はボーア半径と水素原子から出る光のスペクトル波長の導出となっているので、必ずできるようにしましょう。
またスペクトル図は、一番左のスペクトル線のかたまりが、m=1の定常状態へ遷移するときに発生する光子の波長(ライマン系列)、左から2番目のスペクトル線のかたまりが、m=2の定常状態へ遷移するときに発生する光子の波長(バルマー系列)、左から3番目のスペクトル線のかたまりが、m=3の定常状態へ遷移するときに発生する光子の波長(パッシェン系列)を表しているということをまず理解しましょう。
スペクトル線のかたまりの中で一番右側が、n=m+1からmへの遷移で(波長が大きい=発生するエネルギーが小さい)、一番左側がn=∞からmへの遷移(波長が一番小さい=発生するエネルギーが大きい)ということになります。
(4)必要な知識
①物質波(ド・ブロイ波)の波長

②水素原子のスペクトル

③ボーアの量子条件
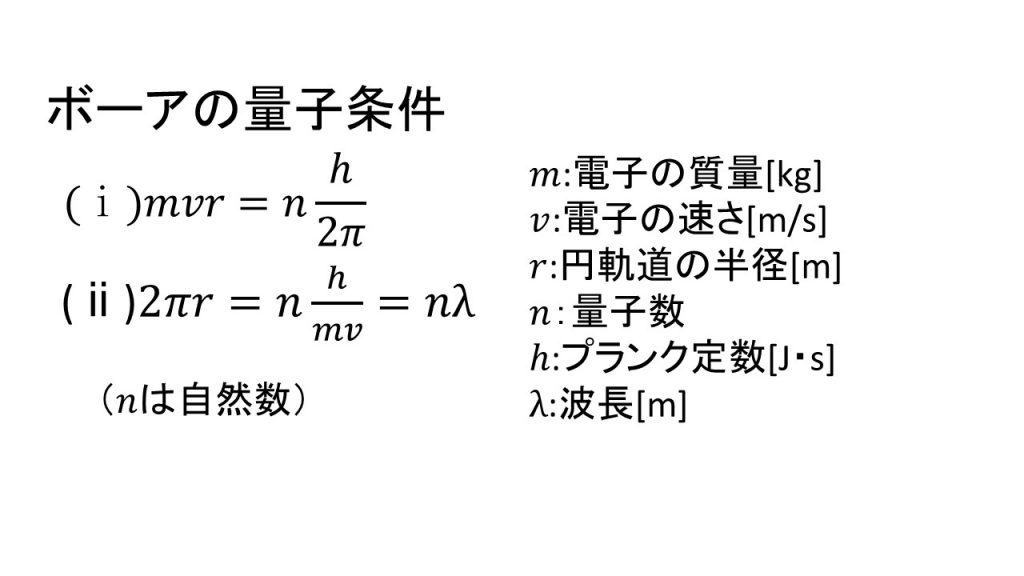

④ボーアの振動数条件

☆式の意味:エネルギーの異なる他の軌道に移るとき、2つの軌道のエネルギーの差を光子として放出または吸収する。
⑤ボーア半径
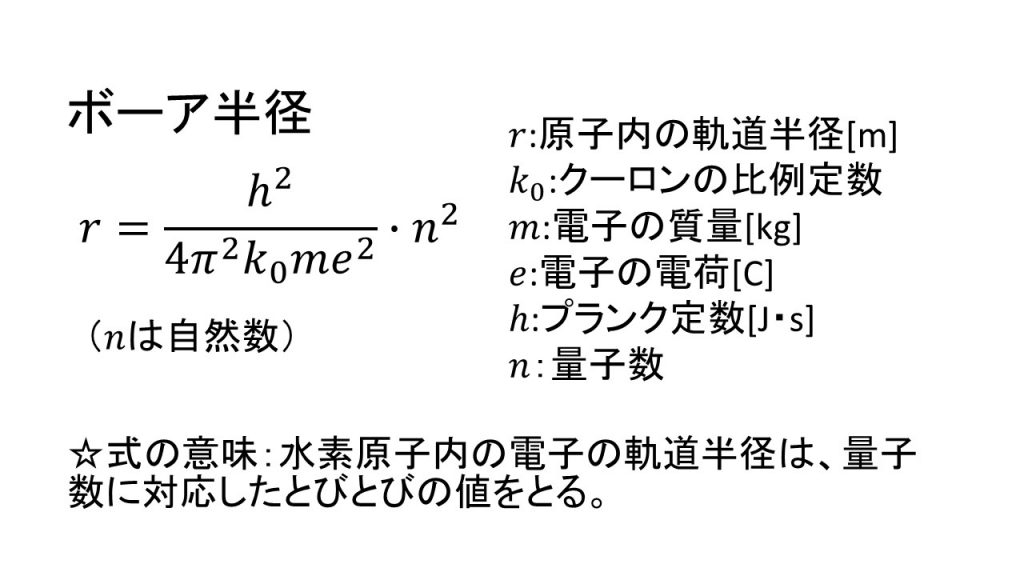
⑥水素原子のエネルギー準位
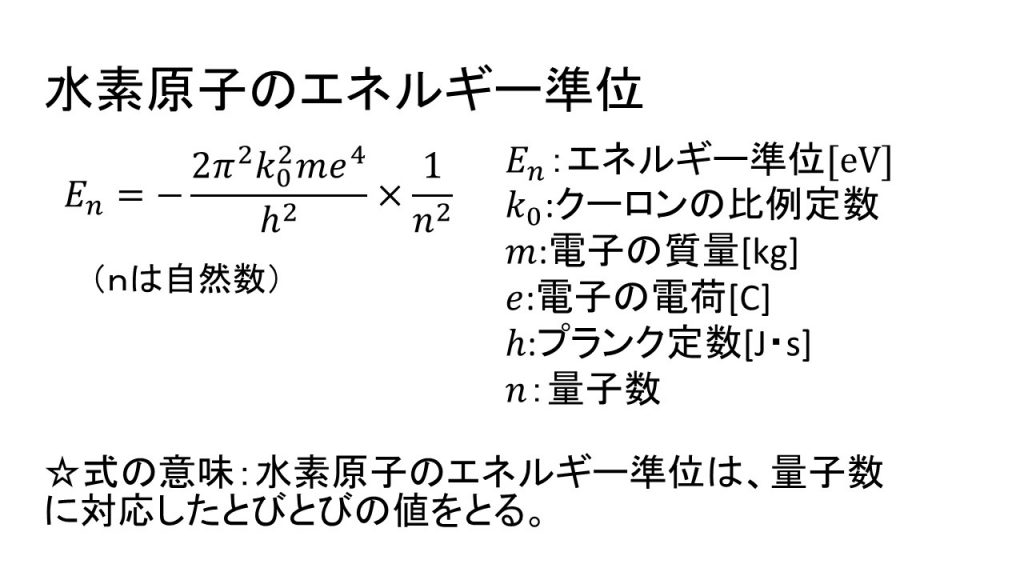
※②⑤⑥は覚える必要はないが、式の形と導出の仕方は知っておきましょう。
